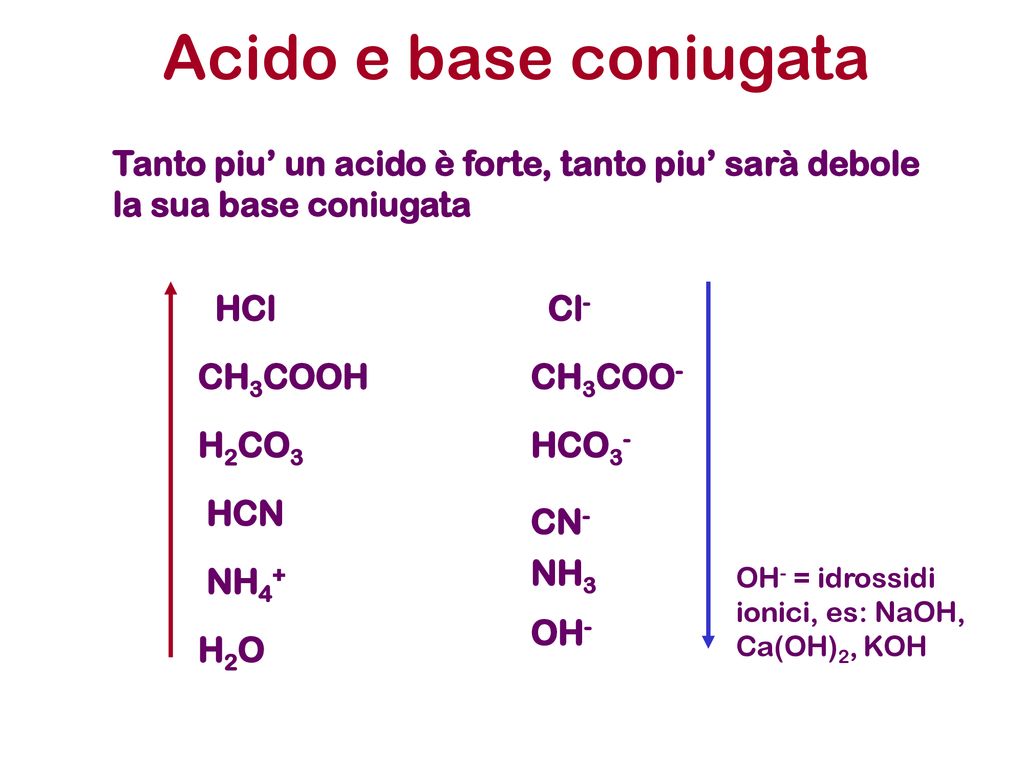
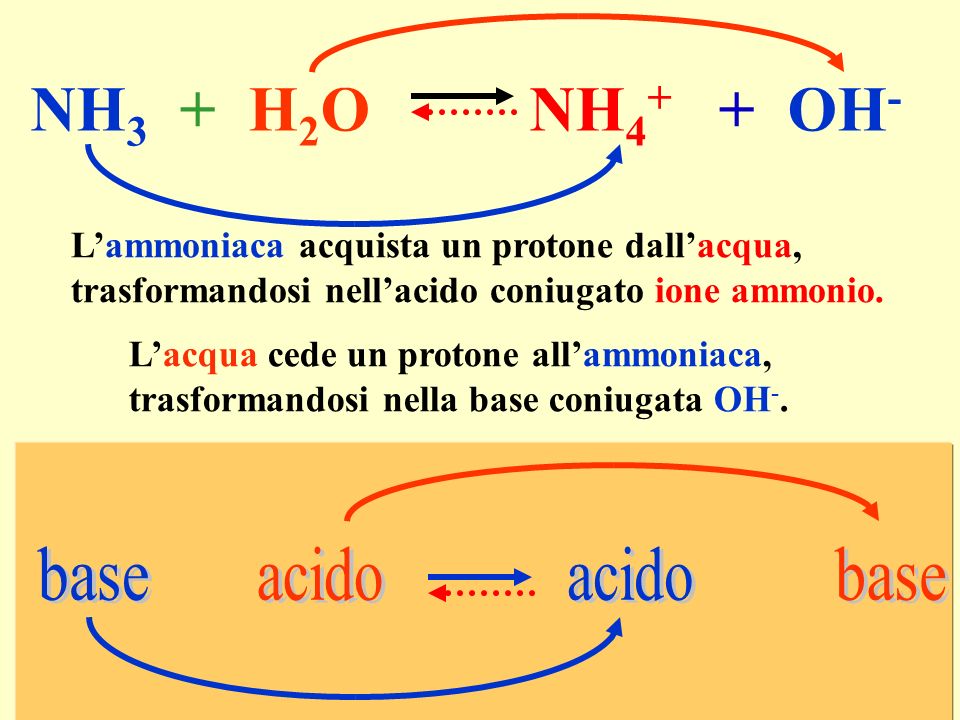
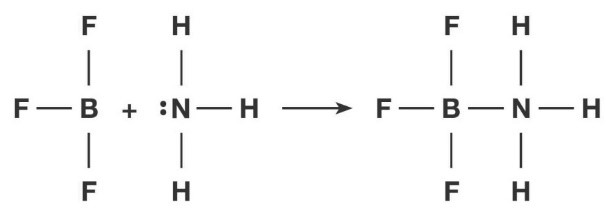
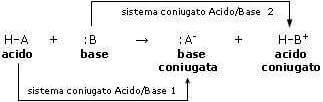
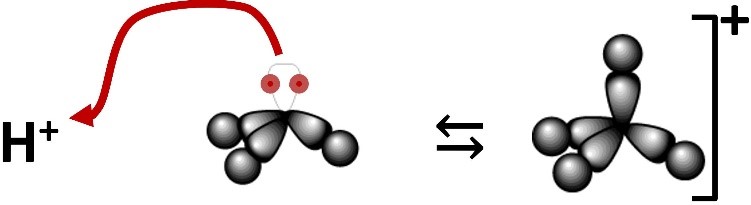
SOLUZIONE TAMPONE | SOLUZIONE TAMPONE Si definisce una soluzione tampone una soluzione che si oppone alla variazione del pH per aggiunte moderate di acidi o basi. Si... | By Chimica Applicata | Facebook

D7-1 La costante di dissociazione ionica dell'ammoniaca in acqua è uguale a 1.8·10-5. Determinare (a) il grado di dissociazione e (b) la concentrazione. - ppt scaricare

PPT - Al punto equivalente le moli di acido e di base sono uguali. PowerPoint Presentation - ID:6947148

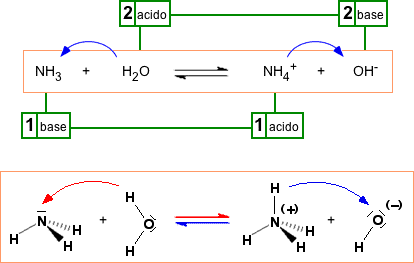
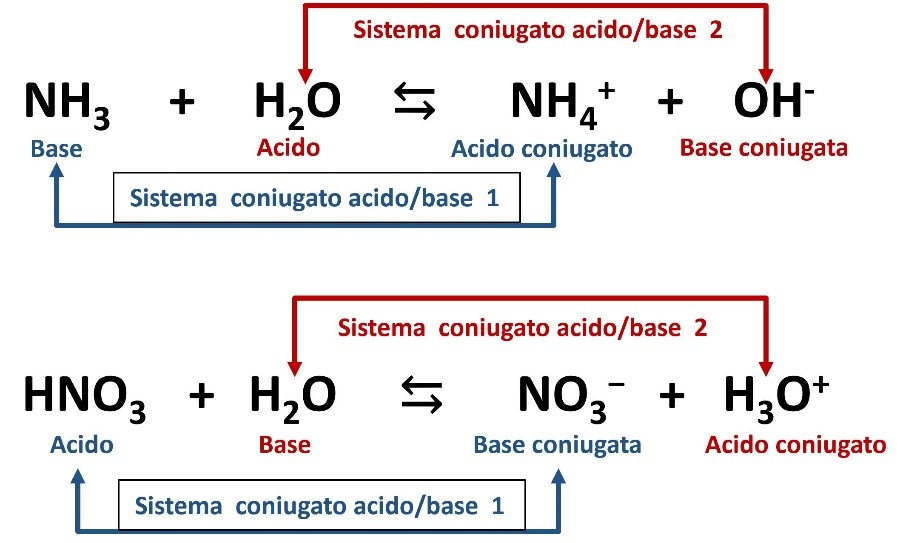
Acidi e basi - Una prima definizione di acidi e basi è dovuta adArrhenius(1890): Acido: composto che - Studocu
I principi e la pratica della chirurgia. Acido urico tartaro. Urato di cristalli di ammoniaca. La presenza di acido urico nei sedimenti, ghiaia, o un calcolo, può bedetermined trattando una piccola
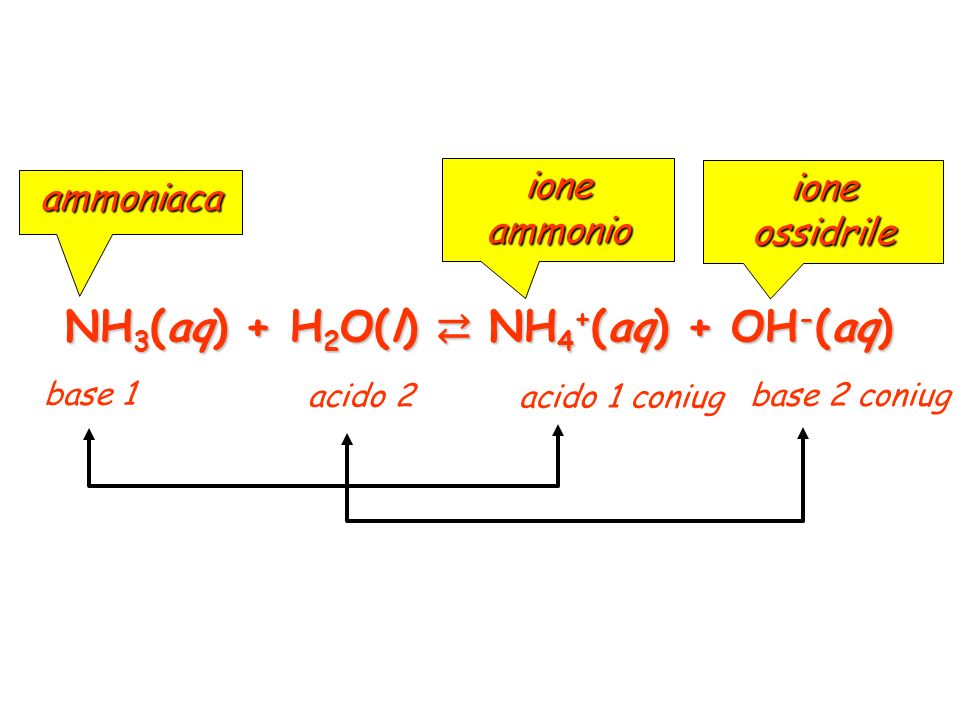
Acidi e Basi. Acido è una parola che deriva dal latino “acetum” (aceto). Col tempo la parola si è estesa a tutte le sostanze che hanno un sapore “acidulo”. - ppt scaricare

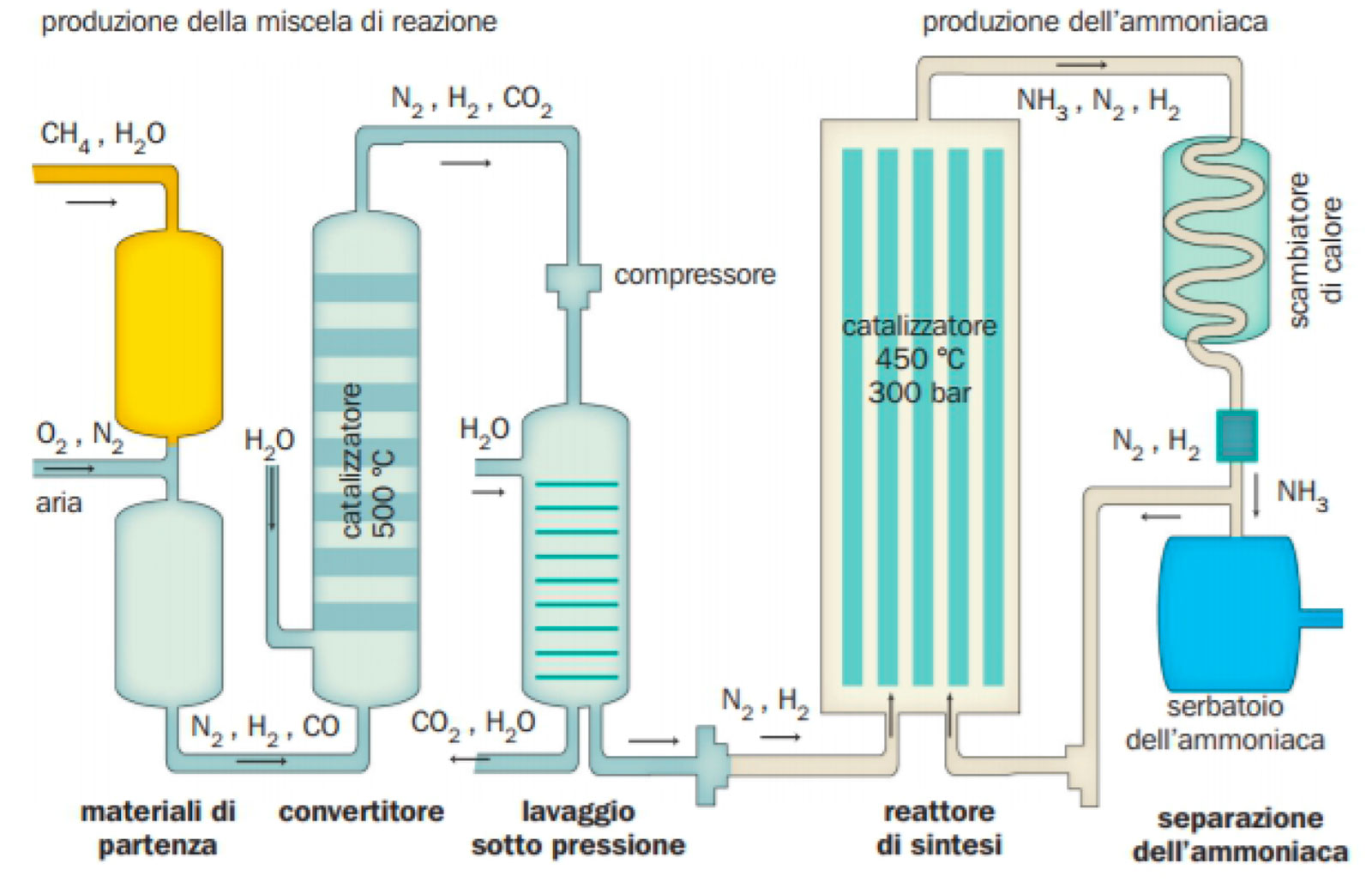
. La chimica dell'agricoltura, per gli studenti e gli agricoltori. Chimica agraria. 214 CONCIMI AZOTATI di nitrurazione, l'ammoniaca viene trasformata in acido nitrico e acido solforico è libera. Entrambi gli acidi richiedono basi che li neutrahze, e quindi vi è il ...